Saúde
Técnico manipula dose de vacina da Pfizer no Centro de Pesquisa Clínica da OSID, em Salvador (BA)

Pfizer e BioNTech solicitam uso emergencial de vacina contra Covid-19 à União Europeia
Reguladora de medicamentos da UE anuncia que concluirá revisão dos dados do imunizante candidato das companhias em 29 de dezembro
FRANKFURT — A farmacêutica americana Pfizer e o laboratório de biotecnologia alemão BioNTech soilicitaram ao regulador de medicamentos da Europa autorização para o uso emergencial de sua vacina contra a Covid-19 no continente, informaram as empresas nesta terça-feira. As duas companhias submeteram anteriormente pedidos semelhantes nos Estados Unidos e no Reino Unido e, na última semana, divulgaram que seu imunizante candidato é 95% eficaz contra o novo coronavírus.
Diversidade: Casais do mesmo sexo vão à Justiça para ter representatividade sobre seus filhos
O pedido para a Agência Europeia de Medicamentos (EMA) vem depois de as empresas pedirem aprovação nos EUA em 20 de novembro, deixando-as um passo mais perto de lançarem sua vacina. O pedido feito na Europa conclui o processo de análise contínua, que foi iniciada junto à EMA em 6 de outubro.
“Se a EMA concluir que as vantagens da vacina candidata superam seus riscos de proteção contra a Covid-19, recomendará a concessão de uma CMA (autorização condicional) que poderia permitir o uso do BNT162b2 na Europa antes do final de 2020”, informa o comunicado.
Ao lado da americana Moderna, a aliança Pfizer/BioNTech é a primeira a submeter oficialmente sua solicitação de comercialização à autoridade sanitária da UE.PRINCIPAIS VACINAS EM TESTE CONTRA A COVID-191 de 5
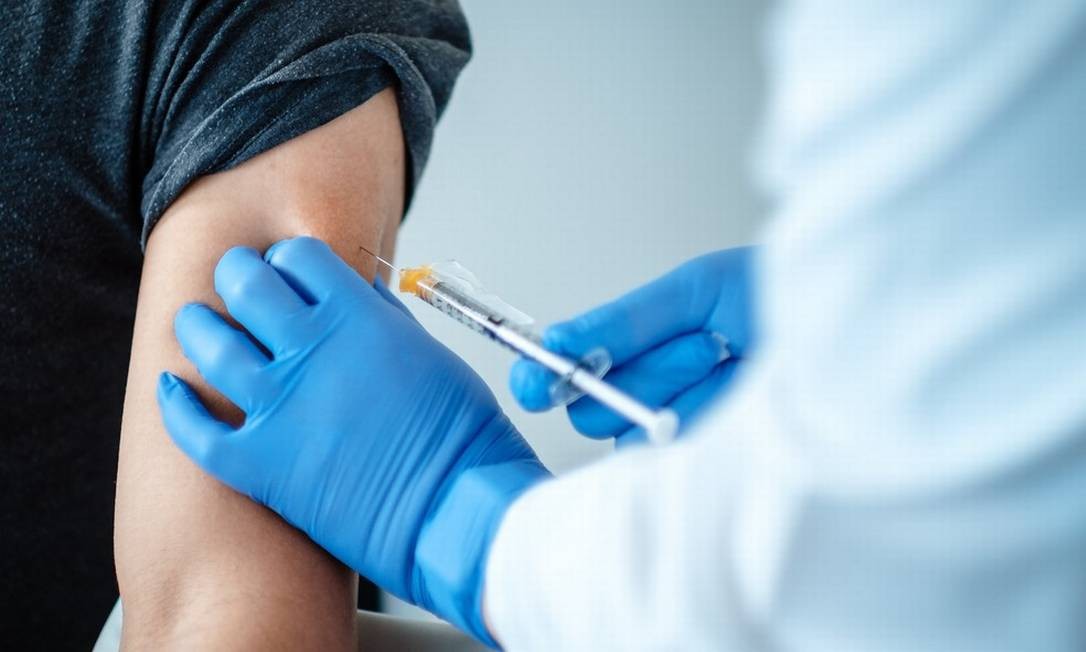

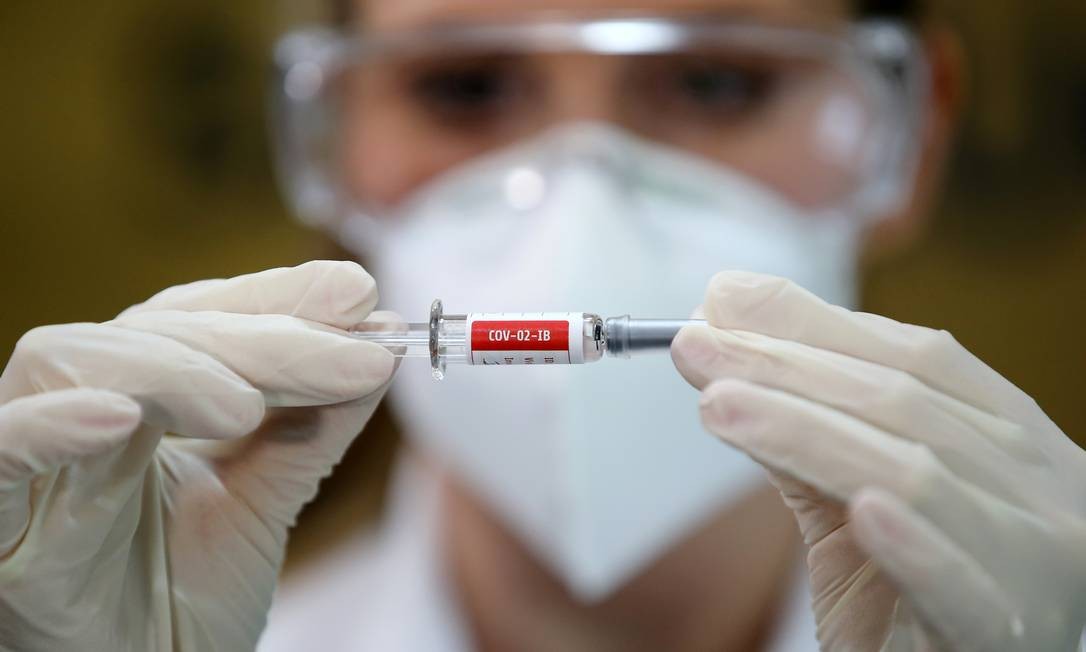
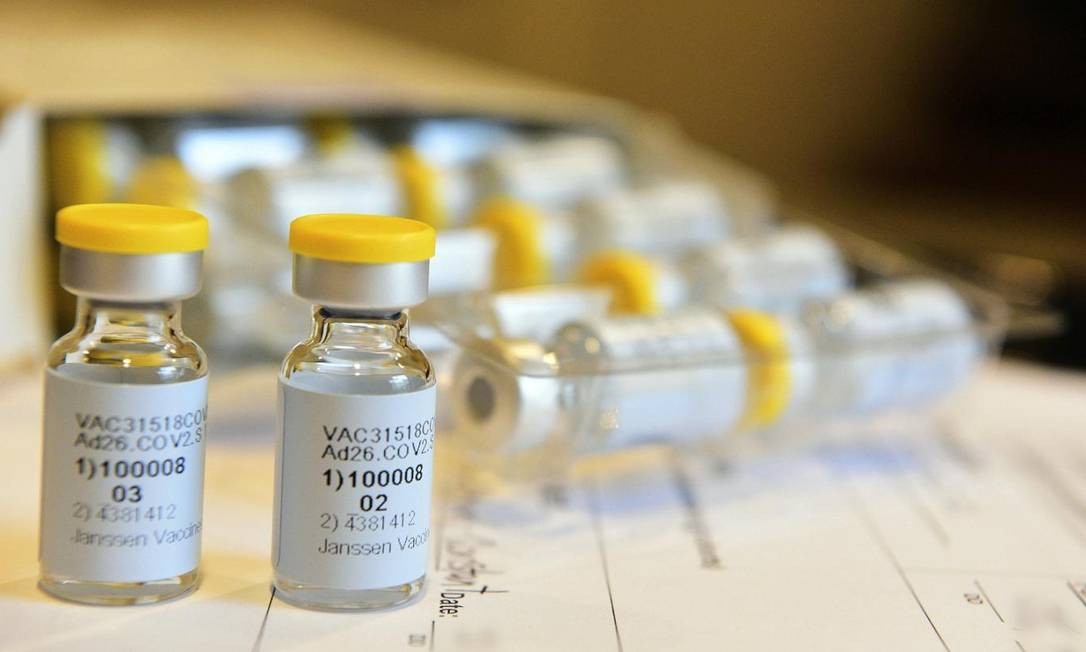
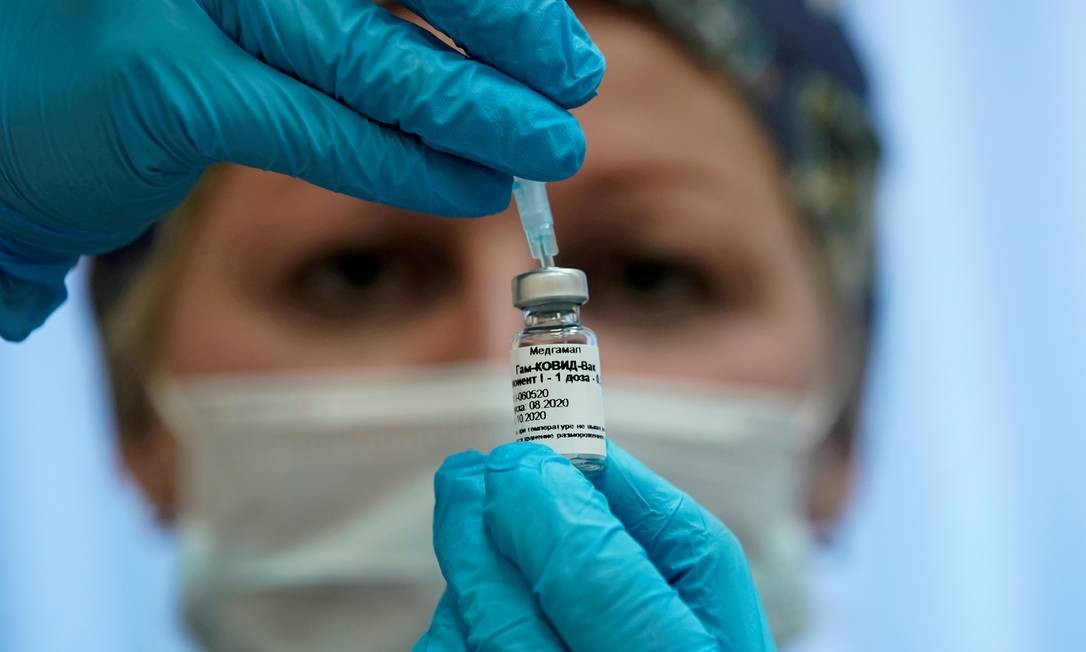
Margareth Dalcolmo: Muitas perguntas, poucas respostas
Apesar da expectativa, a EMA afirmou na sequência do comunicado da farmacêutica que a agência completará o processo de revisão da Pfizer em 29 de dezembro. O da Moderna, por sua vez, ficará para 12 de janeiro.
A norte-americana Pfizer e a alemã BioNTech anunciaram o resultado final dos testes com sua vacina em 18 de novembro, mostrando que sua candidata é 95% eficaz na prevenção da Covid-19, sem preocupações de segurança relevantes, levantando a perspectiva de uma aprovação nos EUA e na UE em dezembro.
O governo britânico informou na semana passada que a parceria entre a norte-americana e a alemã relatou dados de seus testes clínicos para a Agência Regulatória de Medicamento e Saúde do Reino Unido (MHRA).
Com sede em Amsterdã, a Agência Europeia de Medicamentos é responsável por autorizar e controlar os remédios na União Europeia. A aprovação final, dada pela Comissão Europeia, permite aos laboratórios comercializar os seus medicamentos em todos os países da UE.
Entrevista: ‘Brasil terá menos casos do que no pico, mas o suficiente para colapsar o sistema’, diz especialista da UFRJ
Para examinar os dados de segurança e eficácia das vacinas contra a covid-19 à medida que se tornam disponíveis, a EMA implementou um procedimento acelerado denominado “revisão contínua”, como também fez a Anvisa no Brasil. As vacinas da Pfizer/BioNTech, Moderna e Oxford/AstraZeneca são os três projetos de vacinas submetidos há várias semanas a esta “revisão contínua”.
Esperadas no mercado até o fim do ano, os imunizantes da Pfizer/BioNTech e Moderna são baseados na tecnologia de RNA mensageiro, e seriam as primeiras vacinas licenciadas da História com essa nova tecnologia.
A vacina Pfizer/BioNTech já está sendo avaliada nos EUA pela Agência de Alimentos e Medicamentos (FDA) e poderá ser autorizada no país logo após 10 de dezembro.
O Globo e agências internacionais









































